限制性内切酶在特定识别位点切割DNA的特性,使得这些酶在分子生物学技术中成为必不可少的核心工具。其可在分子克隆、mRNA转录模板制备、基因定位和分离等等应用领域发挥重要作用。近年来,以病毒包装为基础的基因治疗技术以及mRNA技术,逐渐在新型疗法中凸显出来。其中病毒包装中的质粒构建和mRNA转录中的模板制备均需要无动物源性限制性内切酶的引入使用。
继BspQI、BsaI、XbaI及PmeI后,近岸蛋白再添无动物源性NotI及HindIII限制性内切酶。
识别位点
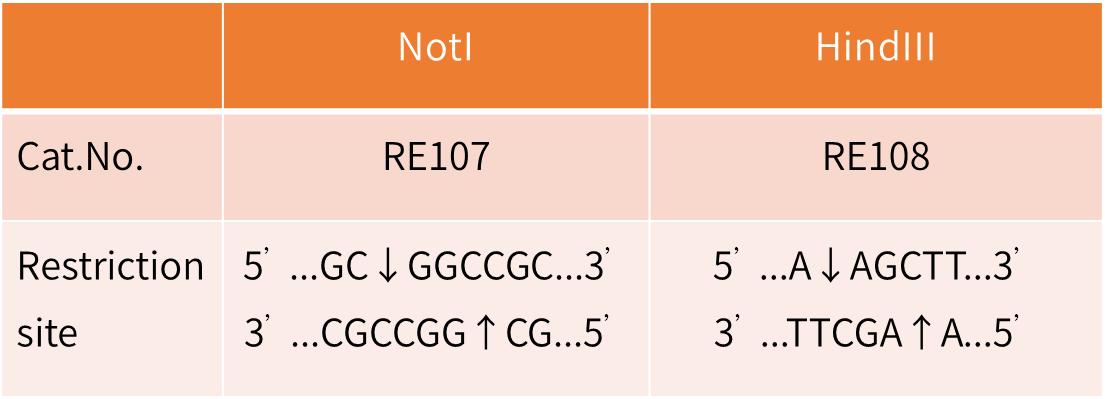
产品特点
高效切割含特异性位点质粒底物
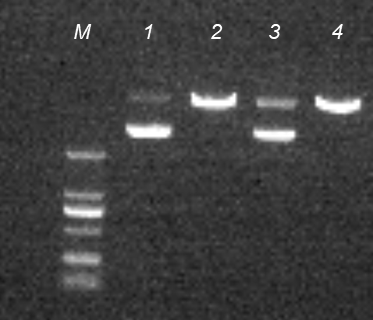
M:DNA Marker 1/3:阴性 2:品牌A 4:Novoprotein
50μl反应体系中,10U不同品牌NotI与1µg质粒进行酶切,37℃孵育1h,质粒被完全线性化。
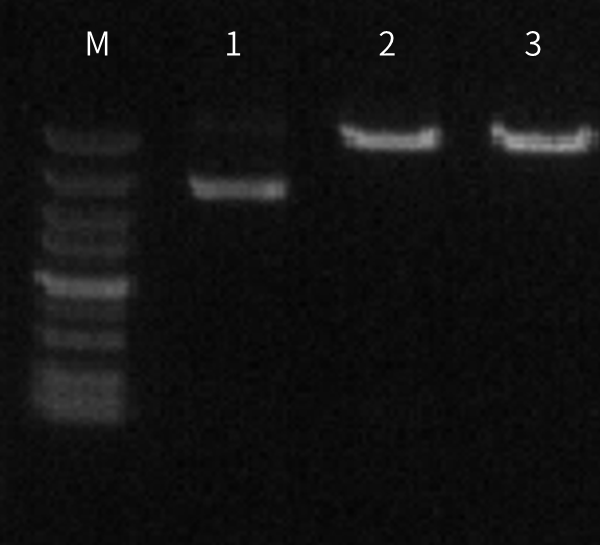
M:DNA Marker 2:品牌A 4:Novoprotein
50μl反应体系中,10U不同品牌HindIII与1µg质粒进行酶切,37℃孵育1h,质粒被完全切割。
无非特异性核酸内切酶活性
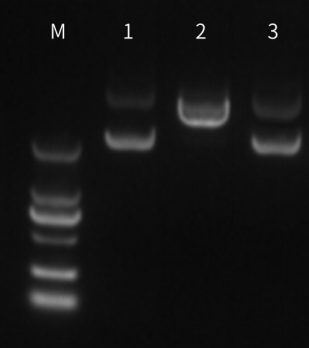
M:DNA Marker 1:阴性 2:品牌A 3:Novoprotein
50μl反应体系中,100U过量不同品牌NotI与1µg无NotI酶切位点的质粒混合,37℃孵育3h,Novoprotein NotI无明显非特异性内切酶活性,而品牌A产生了明显的非特异性切割。
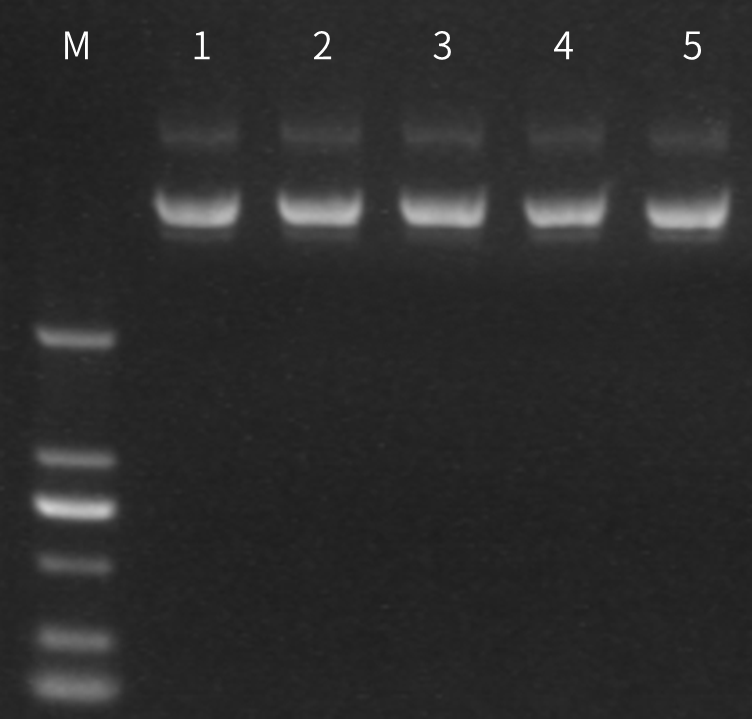
M:DNA Marker 1:阴性 2/3:品牌A(添加量20U/100U) 4/5:Novoprotein(添加量20U/100U)
50μl反应体系中,分别用20U和100U过量不同品牌HindIII与1µg无HindIII酶切位点的质粒混合,37℃孵育3h,无明显非特异性内切酶活性。
无非特异性核酸外切酶活性
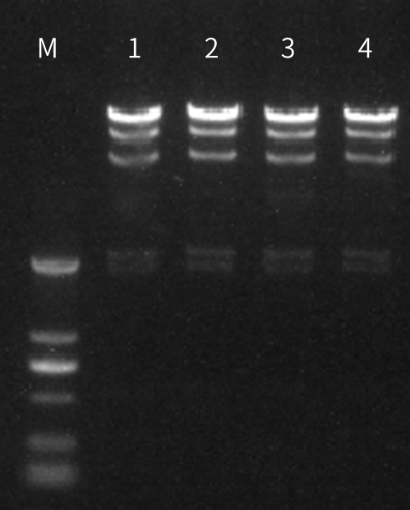
M:DNA Marker 1:阴性 2:品牌A(添加量20U) 3/4:Novoprotein(添加量20U/100U)
50μl反应体系中,分别用20U和100U过量不同品牌NotI与1µg λ HindIII DNA混合,37℃过夜孵育,无明显非特异性外切酶活性。
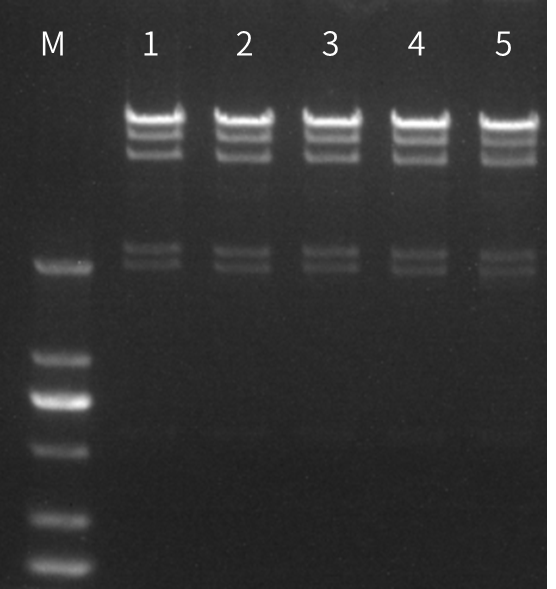
M:DNA Marker 1:阴性 2:品牌A(添加量20U) 3/4/5:Novoprotein(添加量10U/20U/100U)
50μl反应体系中,分别用10U、20U和100U不同品牌HindIII与1µg λ HindIII DNA混合,37℃过夜孵育,无明显非特异性外切酶活性。
更多主流限制性内切酶还有酶切后形成5’末端突出结构或平末端结构的XbaI酶和PmeI。以及IIS型限制性内切酶BspQI、BsaI,其酶切位点在识别位点以外,酶切后可将mRNA的Poly A结构直接暴露在3’端而不产生冗余的酶切位点残基,从根本上杜绝多余碱基造成的不确定性。
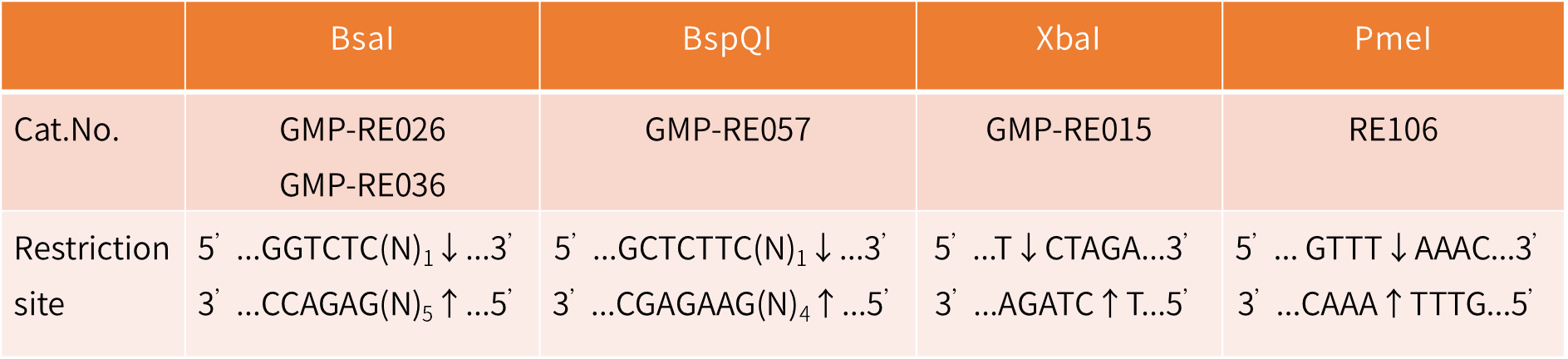
近岸蛋白在推动生物药研发生产过程中不断探索创新,GMP级限制性内切酶BsaI、BspQI和XbaI,无动物源性PmeI、NotI及HindIII,为客户提供更多的酶切位点选择。
